Чи завершать коли-небудь періодичну таблицю елементів

Автор фото, AFP via Getty Images
- Author, Софі Абдулла
- Role, BBC World Service
- Час прочитання: 5 хв
Востаннє періодична таблиця елементів оновлювалася десять років тому. Своє місце в ній знайшли елементи 113, 115, 117 та 118. А міжнародний наглядовий орган у галузі хімії наважився на унікальний крок: назвав один з елементів на честь живого фізика.
Юрій Оганесян очолив російсько-американську дослідницьку групу, яка відкрила елемент 118 (оганессон) у 2002 році. Знадобилися роки, щоб підтвердити результати, – елемент є настільки радіоактивним, що було створено лише кілька атомів.
Можна задатися питанням: чому за 10 років з того часу не додали жодного нового елемента, і чи можна коли-небудь вважати періодичну таблицю завершеною?
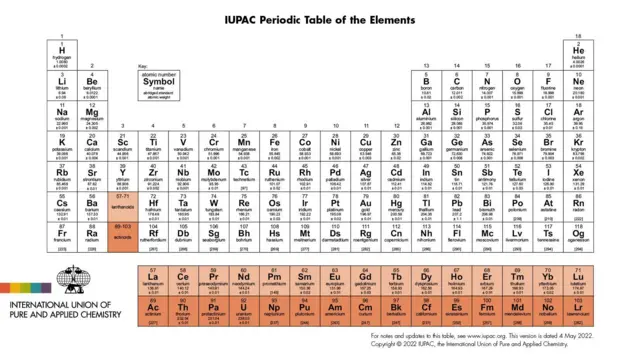
Автор фото, International Union of Pure and Applied Chemistry (IUPAC)
Що таке періодична таблиця
Періодична таблиця — це, по суті, карта хімічних елементів з безліччю квадратів, заповнених їхніми абревіатурами, також відомими як хімічні символи. Її постійно перемальовують.
Елемент — це чиста речовина, що складається лише з одного типу атомів. Атоми є основними будівельними блоками матерії та мають ядро, яке зазвичай містить позитивно заряджені протони та незаряджені нейтрони, оточене негативно зарядженими електронами. З елементів періодичної таблиці складається усе, що ми знаємо у Всесвіті, включно із нами самими.
Ще на початку 1800-х років відкрили багато елементів, але вони не були систематизовані. Кілька вчених прагнули змінити це.
Одним з них був британський хімік Джон Ньюлендс. Він упорядкував елементи за атомною вагою (мірою ваги атома) і побачив, що кожен восьмий має подібні властивості. Наприклад, літій, натрій і калій розташовані за вісім позицій одна від одного та демонструють схожі реакції з водою. Він назвав це законом октав.

Автор фото, Oxford Science Archive/Print Collector via Getty Images
Російський хімік Дмитро Менделєєв, якого називають батьком періодичної таблиці, взяв ідею повторюваних властивостей і сформулював її в так званий періодичний закон.
У 1869 році він створив основу для сучасної періодичної таблиці, впорядкувавши елементи за атомною вагою. На відміну від версії Ньюлендса, в його таблиці залишалися прогалини для відсутніх елементів. Його робота набула популярності, коли ці передбачені вченим елементи були пізніше відкриті.
Сьогодні елементи періодичної таблиці визначаються та організовуються за їхнім атомним номером – кількістю протонів у ядрі. Водень має один протон, тоді як оганесон – 118.
Елементи в одному стовпці мають подібні хімічні властивості, наприклад, як вони реагують з іншими речовинами.
Вони часто також мають певну закономірність у своїх фізичних властивостях, таких як температура плавлення, що допомагає вченим передбачити їхню поведінку. Інженери, наприклад, можуть використовувати періодичну таблицю для вибору матеріалів під час проектування мостів та літаків.

Автор фото, Jiojio via Getty Images
Якщо вчений вважає, що він відкрив новий елемент, глобальний наглядовий орган, що називається Міжнародний союз чистої та прикладної хімії (IUPAC), перевіряє його існування, а елемент отримує місце в таблиці. Цей процес може тривати роками.
Вважають, що ми знайшли всі природні елементи на Землі, і вони складають більшу частину таблиці. Важчі елементи можуть бути створені штучно в лабораторії шляхом поєднання двох легших.
Завдяки розвитку технологій вчені змогли додати в таблицю більше надважких елементів. Теоретично люди могли б продовжувати намагатися створювати нові елементи, але це стає дедалі складніше.
Створення нових елементів
Щоб мати змогу поєднати легші елементи разом для створення дедалі важчихнових, "ми повинні залучати все більше енергії, будуючи все більші циклотрони або прискорювачі", пояснює професор Філ Блоуер, керівник кафедри хімії та біології в Королівському коледжі Лондона.
"Оскільки елементи стають все більшими та важчими, вони стають все менш стабільними через протони в ядрі", — каже Блоуер.

Автор фото, San Francisco Chronicle/Hearst Newspapers via Getty Images
Співвідношення протонів і нейтронів у ядрі визначає, чи буде ядро стабільним чи нестабільним. Позитивно заряджені протони природним чином відштовхуються один від одного, але присутність нейтронів може утримувати їх разом.
"Коли ви створюєте все важчі й важчі елементи, ви додаєте більше протонів до ядра, і щоб воно не розпалося, вам потрібна зростаюча кількість нейтронів", – пояснює доктор Чінція Імберті, керівник групи Imaging Metallomics у Королівському коледжі Лондона.
Елемент може існувати з різною кількістю нейтронів – ці варіації називаються ізотопами. Нестабільні ізотопи є радіоактивними – вони розпадаються, випромінюючи радіацію.
Автор фото, KTSDESIGN/Science Photo Library via Getty Images
Як дізнатися головне про Україну та світ?
Підписуйтеся на наш канал тут.
Кінець Whatsapp
"Усі елементи, важчі за свинець (елемент 82), є радіоактивними, вони за своєю суттю нестабільні та розкладаються", – пояснює доктор Джонатан Рурк, хімік з Університету Кардіффа та почесний професор Університету Ворвіка у Великій Британії.
"Якби ми змогли створити один атом одного з цих елементів, він би недовго проіснував", – пояснює він.
Це особливо стосується елементів, починаючи з номера 100 (фермій) і далі.
"Ви створюєте кілька атомів, і можете трохи знати про їхні фізичні властивості. Але вони не мають жодного практичного застосування", – пояснює доктор Імберті.
Тим не менш, пошуки наступних елементів, які додали б у періодичну таблицю новий рядочок, тривають. Багато спроб знайти числа 119 та 120 поки що не увінчалися успіхом, але різні дослідницькі групи продовжують спроби.
Вчені кажуть, що дослідження елементів на крайніх рівнях може дати нам нове розуміння того, як працюють атоми, межі атомних ядер та можливість перевірити теорії ядерної фізики.
"Потрібно думати не лише про те, чи зможемо ми це створити, — каже Імберті, — але й про те, чи зможе воно прожити достатньо довго, щоб ми могли відкрити його в осмисленому сенсі, дізнатися трохи про нього... перш ніж воно зникне".






















