Нобелевскую премию по химии присудили за разработку новых металлоорганических соединений. Они могут стать «материалом XXI века»

Автор фото, Niklas Elmehed © Nobel Prize Outreach
- Автор, Отдел новостей
- Место работы, Русская служба Би-би-си
Нобелевскую премию по химии присудили за разработку новых металлоорганических соединений. Ее разделили японец Сусуми Китагава, британец Ричард Робсон и иорданец Омар М. Яги.
Ученые создали молекулярные конструкции с большими пространствами, через которые могут проходить газы и другие химические вещества. Эти конструкции, так называемые металлоорганические каркасы, могут использоваться для сбора воды из воздуха в пустыне, улавливания углекислого газа, хранения токсичных газов или катализа химических реакций, говорится в пресс-релизе Нобелевского комитета.
Сусуму Китагава родился в 1951 году в Киото. Получил докторскую степень в Университете Киото в 1979 году, профессор этого университета.
Ричард Робсон родился в 1937 году в британском Гласберне. Докторскую степень получил в 1962 году в Оксфордском университете, он профессор Мельбурнского университета.
Омар М. Яги родился в 1965 году в Аммане. В 1990 году получил докторскую степень в Университете Иллинойса в Урбана-Шампейне. Профессор Калифорнийского университета в Беркли.
Сусуму Китагава, Ричард Робсон и Омар Яги разработали новую форму молекулярной архитектуры. В их конструкциях ионы металлов функционируют как узлы, соединенные длинными органическими молекулами на основе углерода. Вместе ионы металлов и молекулы организованы так, что образуют кристаллы, содержащие большие полости. Эти пористые материалы называются металлоорганическими каркасами (metal-organic frameworks, MOF). Изменяя строительные блоки, используемые в MOF, химики могут конструировать их таким образом, чтобы они могли улавливать и хранить определенные вещества. MOF также могут вызывать химические реакции или проводить электричество.
«Металлоорганические каркасы имеют огромный потенциал, открывая невиданные ранее возможности для создания материалов с новыми функциями на заказ», — сказал Хайнер Линке, председатель Нобелевского комитета по химии.
Металлоорганические кристаллы как «материал XXI века»?
В 1974 году Ричард Робсон, преподающий в Мельбурнском университете в Австралии, получил задание сделать из деревянных шариков модели атомов, чтобы студенты могли создавать молекулярные структуры. Он просверлил в них отверстия, чтобы к атомам можно было прикрепить деревянные стержни — химические связи. Однако отверстия нельзя было размещать случайным образом. Каждый атом — например, углерод, азот или хлор — образует химические связи определенным образом. Робсону нужно было отметить, где следует просверлить отверстия.
Тут мы публикуем только главные новости и самые интересные тексты. Канал доступен для нероссийских номеров.
Подписывайтесь
Конец истории Реклама WhatsApp-канала
Он попробовал построить несколько молекул и понял: в расположении отверстий заложен огромный объем информации. Модели молекул автоматически приобретали правильную форму и структуру благодаря расположению отверстий. Робсон заинтересовался, что произойдет, если воспользоваться свойствами атомов, чтобы соединить между собой различные типы молекул, а не отдельные атомы.
Он начал с очень простой модели, опираясь на структуру алмаза, в которой каждый атом углерода связывается с четырьмя другими, образуя пирамиду. Робсон хотел построить похожую структуру, но на основе положительно заряженных ионов меди Cu+. Как и углерод, они предпочитают иметь вокруг себя четыре других атома.
Он соединил ионы меди с молекулой тетрацианотетрафенилметана, имеющей четыре «руки». На конце каждой «руки» молекула содержала химическую группу, нитрил, которая притягивалась к положительно заряженным ионам меди.
В то время большинство химиков полагали, что ионы меди могут соединяться с такими молекулами только в хаотическом порядке. Однако, как и предсказывал Робсон, притяжение ионов и молекул друг к другу сыграло свою роль, и они сложились в крупную молекулярную конструкцию, образовав правильную кристаллическую структуру. Однако, в отличие от компактного алмаза, в этом кристалле было множество огромных полостей.
В 1989 году Робсон опубликовал свою работу в Журнале Американского химического общества, а через год представил несколько новых типов молекулярных конструкций с полостями, заполненными различными веществами. Одну из них он использовал для обмена ионами. Он погрузил заполненную ионами конструкцию в жидкость, содержащую ионы другого типа. В результате ионы поменялись местами, продемонстрировав, что вещества могут поступать в конструкцию и выходить из нее.
В своих экспериментах Робсон показал, что такой рациональный дизайн можно использовать для создания кристаллов с просторным внутренним пространством, оптимизированным для конкретных химических веществ. Однако конструкции Робсона были довольно хрупкими и имели тенденцию разваливаться.
Сусуму Китагава начал исследовать возможности создания пористых молекулярных структур, не считая, что они должны иметь конкретное назначение. Когда в 1992 году он представил свою первую молекулярную конструкцию, она не несла особо полезных функций, но продемонстрировала новый подход к проблеме. Как и Робсон, Китагава использовал ионы меди в качестве узлов, которые были соединены между собой более крупными молекулами.
В 1997 году исследовательская группа Китагавы создала трехмерные металлоорганические каркасы, пересекаемые открытыми каналами, используя ионы кобальта, никеля или цинка и молекулы бипиридина. Когда они высушили один из этих материалов, удалив из него воду, он оказался стабильным, а пространства между его элементами можно было даже заполнить газами. Материал мог поглощать и выделять метан, азот и кислород, не меняя формы.
Китагава также понял, что MOF могут образовывать мягкие материалы. В отличие от уже доступных химикам пористых материалов, цеолитов, которые создаются из диоксида кремния и обычно являются твердыми материалами, MOF содержат гибкие молекулярные строительные блоки, и из них можно делать гибкий материал.
В 1992 году Омар Яги в Университете штата Аризона попытался использовать рациональный дизайн для соединения различных химических компонентов, чтобы создать большие кристаллы. В 1995 году Яги опубликовал структуру двух различных двумерных материалов; они были похожи на сетки и скреплялись медью или кобальтом. Пустые пространства одного из них можно было заполнить молекулами других веществ, и он был настолько стабилен, что выдерживал нагрев до 350°C, не разрушаясь.
Яги установил следующую веху в развитии металлоорганических каркасов в 1999 году, когда представил миру MOF-5. Этот материал стал классическим в своей области. Он представляет собой исключительно просторную и стабильную молекулярную конструкцию. Даже в пустом состоянии его можно нагревать до 300 °C без разрушения.
Но главное достоинство MOF-5 — это огромная площадь, скрывающаяся внутри кубических пространств материала. Пара граммов MOF-5 вмещает площадь, равную футбольному полю, а это означает, что он может поглощать гораздо больше газа, чем цеолит.
В двух статьях, опубликованных в журналах Science и Nature в 2002 и 2003 годах, Яги показал, что MOF можно модифицировать и изменять рациональным образом, придавая им различные свойства. Например, один из вариантов MOF-5 мог хранить огромные объемы метана, который, по мнению Яги, можно было использовать в транспортных средствах, работающих на газе.
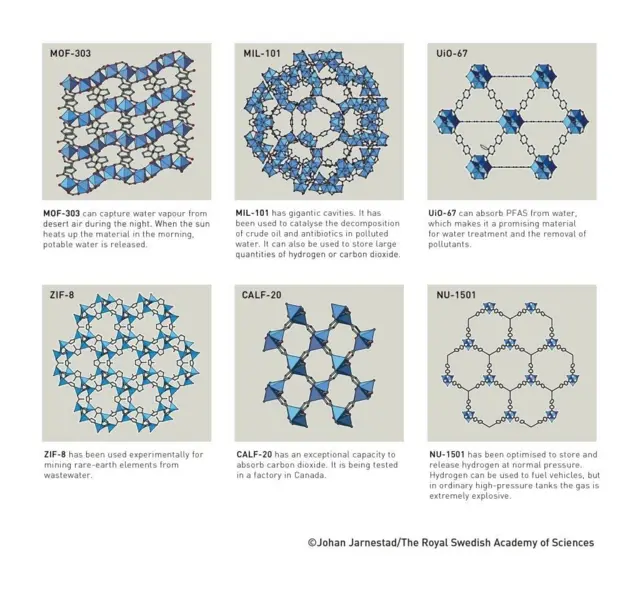
Автор фото, Johan Jarnestad/The Royal Swedish Acafemy of Sciences
Исследователи создали множество различных функциональных MOF. До сих пор в большинстве случаев эти материалы использовались только в небольших масштабах. Чтобы использовать преимущества MOF-материалов, многие компании сейчас инвестируют в их массовое производство и коммерциализацию. Электронная промышленность теперь может использовать MOF-материалы для удержания некоторых токсичных газов, необходимых для производства полупроводников. Другой MOF может разлагать вредные газы, в том числе некоторые, которые могут использоваться в качестве химического оружия. Многие компании также тестируют материалы, которые могут улавливать углекислый газ, производимый заводами и электростанциями, чтобы сократить выбросы парниковых газов.
Среди уже разработанных металлоорганических материалов — MOF-303, который может улавливать водяной пар из воздуха пустыни в ночное время, а днем при нагреве солнечными лучами выделяет пригодную для питья воду; MIL-101, используемый для катализа разложения сырой нефти и антибиотиков в загрязненной воде, его также можно использовать для хранения больших количеств водорода или углекислого газа; ZIF-8, с которым экспериментируют для добычи редкоземельных элементов из сточных вод.
CALF-20 обладает исключительной способностью поглощать углекислый газ. Он проходит испытания на заводе в Канаде.
Некоторые исследователи считают, что металлоорганические каркасы обладают таким огромным потенциалом, что станут «материалом XXI века».
Лауреаты прошлых лет
Лауреатами Нобелевской премии по химии 2024 года стали ученые Дэвид Бейкер, Демис Хассабис и Джон Джампер. Премия присуждена за изучение структур белков.
Американскому химику Дэвиду Бейкеру удалось создать совершенно новые виды белков. А британцы Демис Хассабис и Джон Джампер разработали модель искусственного интеллекта для решения проблемы полувековой давности — предсказания сложной структуры белков.

Автор фото, Getty Images
C 1901 года Нобелевская премия по химии присуждалась 116 раз. Она не присуждалась восемь раз: в 1916-19, 1924, 1933, 1940-42 годах, когда Нобелевский комитет не счел представленные номинантами работы достойными награды.
Из 195 человек, удостоенных Нобелевской премии по химии, восемь женщин. Две из них, Мария Кюри и Дороти Кроуфут Ходжкин, получили премии единолично, без соавторов.
Мария Кюри также получила Нобелевскую премию по физике в 1903 году, а ее дочь Ирен в 1935 году разделила награду с мужем Фредериком Жолио, в 35 лет ставшим самым молодым лауреатом премии по химии.
Самый возрастной лауреат — Джон Б. Гуденаф, он получил Нобелевскую премию по химии в 2019 году в возрасте 97 лет. Этот ученый — самый пожилой лауреат Нобелевской премии во всех дисциплинах. Фредерик Сэнгер и Барри Шарплесс получали Нобелевскую премию по химии дважды.
Адольф Гитлер запретил трем немецким лауреатам Нобелевской премии получать ее — Рихард Кун в 1938 году и Адольф Бутенандт в 1939 году стали лауреатами премии по химии, а Герхард Домагк был удостоен Нобелевской премии по физиологии и медицине в 1939 году. Все они смогли позже получить Нобелевский диплом и медаль, но не деньги.